Начало коррозии проявляется в виде темных точек на корпусе мотолодки , а также серых или беловатых пятен. Наиболее часто коррозия появляется внутри мотолодки , в местах, где скапливается вода, — под пайолами, внутри воздушных отсеков. С наружной стороны корпуса особое внимание следует обратить на днище в районе килевого профиля и в соединении листов обшивки по скуле, т. е. там, где защитные покрытия быстрее всего истираются при эксплуатации, и имеется большое количество заклепок.
Обычно коррозию разделяют на общую и местную. При общей коррозии одновременно разрушается тонкий слой металла по всей площади корпуса. При местной коррозии разрушение происходит на локальных участках поверхности, где вкрапления металла служат анодом, тогда как остальная поверхность состоит из менее активного металла. Поскольку местная коррозия локализуется на небольших участках, она протекает особенно интенсивно и, если не принять соответствующих защитных мер, оканчивается разрушением детали. Наиболее распространенными видами такой коррозии являются контактная и шелевая коррозия.
Анод. Трак. Коррозия лодки и как с ней бороться.
Контактная коррозия
Контактная коррозия возникает при непосредственном соприкосновении двух металлов с разным электрическим потенциалом. Она также возникает и в конструкциях из однородных металлов, если для соединения деталей применена сварка, заклепки или болты. Даже металл сварного шва, незначительно отличающийся по своим электрохимическим свойствам от металла корпуса, может образовать с ним гальваническую пару. Интенсивность контактной коррозии определяется разностью электродных потенциалов соприкасающихся металлов. В такой паре разрушается металл с более отрицательным потенциалом.
Для морской воды, где коррозия проявляется гораздо сильнее, чем в пресной, металлы обладают следующими относительными потенциалами (в вольтах); магниевые сплавы — 1,51; цинк — 1,09; сплавы алюминиево-марганцевые (АМц) и алюминиево-магниевые (АМг) — 0,75; кадмий — 0,73; алюминий — 0,64; железо — 0,55; нержавеющие стали (активные) — 0,53; свинец — 0,51; никель — 0,25; латунь, медь, бронза — 0,22; мед-но-никелевые сплавы — 0,20; нержавеющие стали (пассивные) — 0,15; монель-металл — 0,10; серебро — 0,05; титан + 0,15. Следует учитывать, что для пресной воды относительные потенциалы имеют гораздо меньшие значения, однако положение металлов в ряду по электрохимическим свойствам остается без изменений. Для снижения контактной коррозии необходимо в соединениях использовать пары металлов, близкие по своим потенциалам.
Щелевая коррозия
Щелевая коррозия возникает в узких зазорах, неплотностях соединений, куда затруднен свободный доступ воды, обогащенной кислородом. Металл в таком зазоре становится анодом по отношению к остальной поверхности корпуса и подвергается разрушению. Этому виду коррозии весьма подвержена нержавеющая сталь, стойкость которой обеспечивается благодаря образованию пассивного поверхностного слоя. Разность потенциалов в зазорах между деталями из этого сплава способствует разрушению пассивной пленки.
Чудо средство отмывает алюминий на раз
Щелевая коррозия чаще проявляется в соединениях деталей из хромистых нержавеющих сталей тогда как хромоникелевые сплавы более устойчивы. Тем не менее, при использовании нержавеющих сталей всегда следует избегать всевозможных зазоров и неплотностей в соединениях. Из приведенного списка видно, что титан, благодаря положительному потенциалу, очень стоек к коррозии даже в морской воде, однако является катодом по отношению к большинству металлов, находящихся с ним в контакте. Для увеличения долговечности деталей их лучше всего изготавливать из стали 1Х18Н9Т.
На клепаных корпусах из дюралюминия очагами коррозии чаще всего становятся заклепочные швы. Кроме щелевой коррозии в нахлесте листов и профилей могут интенсивно разрушаться заклепки, особенно если они сделаны из металлов с другим химическим составом, чем корпус и получили сильный наклеп.
В любом случае заклепки разрушаются особенно интенсивно из-за большой разницы в их площади и общей поверхности обшивки. Устанавливать оборудование и дельные вещи на корпусе и палубе из дюралюминия лучше с помощью крепежа из металла с более высоким (ближе к нулевому) потенциалом, чем основной металл. Латунный и медный крепеж использовать нельзя — алюминий быстро разрушается даже в пресной воде или на влажном воздухе. Необходимо также избегать зазоров в соединениях, как между деталями, так и между крепежом и деталью, используя, где можно, уплотняющие прокладки, компаунды и герметики.
Источник: www.katera-lodki.ru
Гальваническая коррозия
Гальваническая коррозия — лишь один из видов коррозийного разрушения металла. Процессы эти, не являются простыми, но общее понимание, избавит от множества дорогостоящих проблем. К тому же, этим воздействиям, подвержены не только приводы двигателей.
Для запуска процесса гальванической коррозии, необходимо, всего лишь, иметь в распоряжении, два разнородных металла, с разными электрическими потенциалами. И, конечно, такого важного посредника-проводника, как морская (в идеале) вода, которая, будет играть роль электролита. Как вы понимаете, у нас с вами, этого в избытке. Поэтому, гальваническую коррозию, чаще называют “морская коррозия”.
Ситуация немного сложней, чем кажется. Ведь, даже два, казалось бы, одинаковых металла, запросто могут иметь в своем составе, разные сплавы. Соответственно, нейтральной парой, назвать их уже будет сложно, потому что, один из них, будет более активным. Да и сама неоднородность металлов, провоцирует гальванокоррозию. Поэтому, к примеру, латунь (сплав меди с цинком) — крайне редко используемый металл в судостроении.
На всех корпусах алюминиевых катеров, поворотно-откидных колонок и подвесных лодочных моторов, ниже ватерлинии, обязательной является установка накладок из цинка, магния или алюминия (только, более активного, конечно), как наименее благородного и наиболее активного металла, в нашей связке, который играет роль анода. Тогда как, алюминий — роль катода. Идентичная, более благородная, пара: алюминий — сталь. Конечно, гальваническая пара, соединена проводником.
Отсюда следует, что стальной гребной винт, будет крайне не равнодушен к вашему алюминиевому катеру, в частности, к поворотно-откидной колонке, без должной защиты.

Работу анода, можно увидеть невооруженным глазом, точнее, последствия его работы. К примеру, части угловой колонки или дейдвуда ПЛМ, через некоторое время нахождения в воде, будут покрыты белесым налетом — оксидом цинка. По своей сути, это — высвобождение электронов, то есть, тот же электрический ток.
При этом, частицы вещества, переносятся с анода к катоду, и мы жертвуем одной частью, что бы сохранить другую. Ну это, если совсем грубо. Зато, всем понятно.
Сама накладка-анод, будет постепенно терять в размере. Однако, неравномерное и молниеносное “исчезновение” анода — может быть (не всегда) признаком наличия так называемых, блуждающих токов. Это относится к электролитической коррозии, но суть остается той же.
Впрочем, в этом случае, анодом может стать уже любая подводная часть вашего любимого катера, имеющая наименьшее сопротивление. В подобной ситуации, ток будет искать кратчайший путь лодка-вода-земля. Самая частая причина — самостоятельное неправильное подключение электрооборудования : холодильников, водяных помп, АКБ и т.д. И отсутствие обслуживания и диагностики бортовых электросетей.
Блуждающие токи — это распространенная проблема причалов и марин. Бывает, конечно, и несоблюдение стандартов электрификации, но, основная проблема связана, все-таки, с заземлением. Заземляющий кабель — это необходимая мера безопасности, при подключении катера или яхты к береговому источнику питания.
Поэтому, стальная яхта, с изношенным корпусом, и ваш алюминиевый катер, запитанные от причала, рядом друг с другом, образуют прекрасную катодно-анодную пару. Не в пользу последнего, разумеется. Такую же роль сыграет и стальная причальная стенка.
Для предотвращения подобных казусов, используется простейшая гальваническая развязка.
Вышеописанные процессы, взяты за основу, так называемой, активной катодной (ICCP) защиты. Этот метод, предполагает выработку тока, который пускается на подавление электрохимической активности и предотвращает появление гальванических пар.
Покраска привода и всех алюминиевых деталей — дело очень хорошее, дающее дополнительную защиту, но требующее постоянного обновления. За этим придется тщательно следить. Особенно, за острыми углами, местами соединений и, само-собой, царапинами и повреждениями. Но, если коррозия началась, окраска проблемного места, без зачистки и грунтовки, не поможет.
Краски — необрастайки, на основе меди, ни в коем случае, нельзя применять для покраски алюминиевых катеров.
Так же, не забывайте, что любой вид коррозии, не покрывается гарантийными обязательствами. А перед установкой нового оборудования, помните, что крепеж, особенно, нержавейка, должен быть изолирован от корпуса.
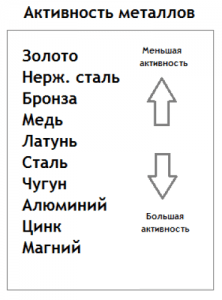
В этой таблице можно легко увидеть, какой, из пары металлов, образующих “батарейку”, будет анодом, а какой — катодом.
Магниевые аноды, лучше оставить для пресной воды. Для морской, следует устанавливать цинковые сплавы или алюминиевые. Главное, подавить желание, установить все три вида протекторов. Тогда магний — станет главным анодом, защищая алюминиевый и цинковый протектор. Надо сказать, что цинковые аноды, постепенно уходят в прошлое, их место занимают теперь, только алюминиевые и магниевые сплавы.

Так или иначе, любой анод требует замены, при сокращении его объема наполовину, дальше, он просто перестанет работать, а в течении его срока службы, необходимо проверять, плотно ли он прилегает к защищаемому металлу.
Ну, и последнее, на протектор, ни в коем случае, нельзя наносить краску, смазку и т.д. Это равносильно его отсутствию.
Источник: spyship.ru
Чипгуру
Здравствуйте форумчане.
Такая проблема-есть детальки из сплава алюминия с многочисленными углублениями и рёбрами обильно покрытыми окислами. Натирать абразивами долго и муторно (много недоступных шкурке мест), пескоструйки естественно нет. Нужно просто привести в божеский вид без фанатизма и полировки.
Из курса школьной химии мы знаем, что оксид алюминия самый стойкий даже к сильным кислотам.
Если сталкивались с такой вещью, чем приводили в эстетический вид поверхности?
Гугл дает пемолюкс, средство Б 52 для снятия краски, некоторые пробовали каустической содой.
Очистка алюминия и сплавов от оксидов
Сообщение #2 Георг Ом » 14 мар 2016, 11:21
Тезка, кипячение в растворе тринатрийфосфата хорошо помогает отъесть и масляно-грязевые пятна и соль с алюминиевых деталей. Только если соль смоет, то под ней корродировавшая поверхность с мутными пятнами так и останется. Всякие щелочи только усугубят дело, и вся поверхность прокорродирует и станет мутной. Всякие дюральки вообще темнеют после щелочей.
Очистка алюминия и сплавов от оксидов
Сообщение #3 ROW » 14 мар 2016, 11:29
На ферме молочные фляги после молочной сыворотки(прокисшего молока до -простокваши (нечто похожее на кефир)) были внутри как новые, правда как долго надо держать в этом растворе алюминий ,не знаю.
Каждый убежден, что другие ошибаются, когда судят о нем, и что он не ошибается, когда судит о других.
Очистка алюминия и сплавов от оксидов
Сообщение #4 AnSm » 14 мар 2016, 11:33
Источник: chipgu.ru